|
|
Cranioplastica |

|

|
|
 
|
|
Chirurgia:
utile da sapersi
B. Zanotti,
T. Ius
Rottura della cranioplastica durante la manipolazione chirurgica
Ogni manufatto su misura in idrossiapatite porosa viene fornito con un “muletto”, vale a dire che i pezzi di cranioplastica sono due, del tutto identici. Se la frantumazione è grave non resta che sostituire il pezzo. Se invece la cranioplastica risulta solo scheggiata, la si può riparare fissando i pezzettini mobili con una goccia di Tissucol® in superficie (no lungo il perimetro di giustapposizione protesi-osso). Se l’ammanco è più consistente, si possono usare dei granuli di idrossiapatite
(Figure 1), miscelati con sangue fresco del Paziente (Figure 1).
Se la frattura è lineare, ben composta, non necessariamente il manufatto va sostituito.
|

|
|
|
|
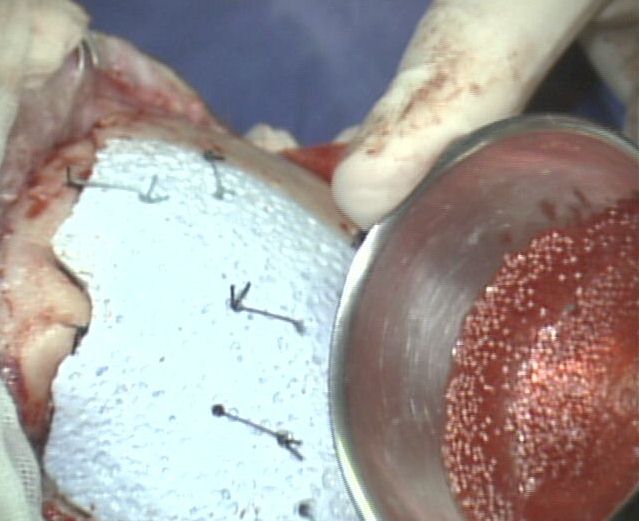
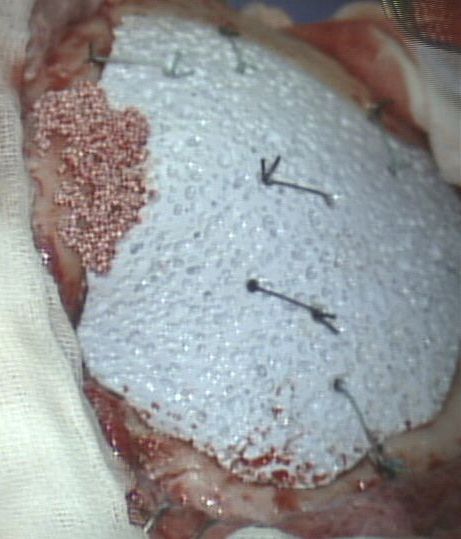
Figura
1. Idrossipataite in granuli. Si tratta di un granulato
sferico caratterizzato da microporosità interconnessa variabile
da 5 a 50 µm che viene impiegato nel riempimento di piccole
cavità secondarie a patologie ossee o traumatiche. Utile anche
nelle rifiniture ai bordi delle cranioplastiche. Al centro
amalgama dei granuli di idrossiapatite con qualche ml di sangue.
Piccola soluzione di continuo fra teca cranica e cranioplastica.
Il cratere è stato riempito con i granuli di idrossiapatite. |
Raccolta ematica extradurale
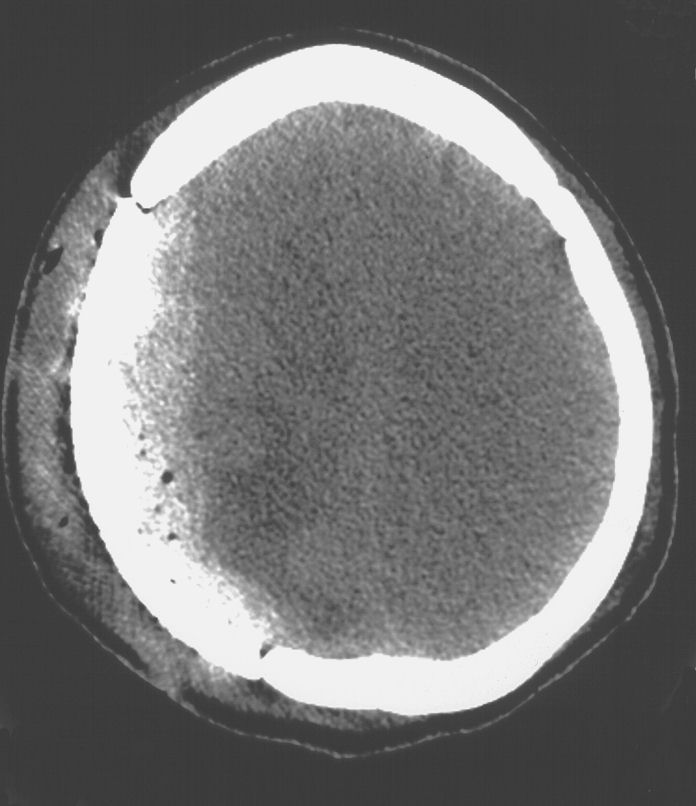
Per mancanza di sostanza cerebrale o per iniziale anelasticità parenchimale dovuta a mesi d’introflessione cutanea nella breccia, può succedere che la dura non sempre e non prontamente possa essere sospesa fino ad aderire alla superficie interna della protesi. Può così accumularsi del sangue fra dura e manufatto, fin quasi a mimare un ematoma extradurale (Figura 2) con, alle volte, apparente dignità chirurgica.
Di fatto, non si tratta mai di un reale espanso sotto pressione, lo stravaso riempie solo uno spazio ex-vacuo. Non si assiste a compressione parenchimale né a dislocazione della linea mediana.
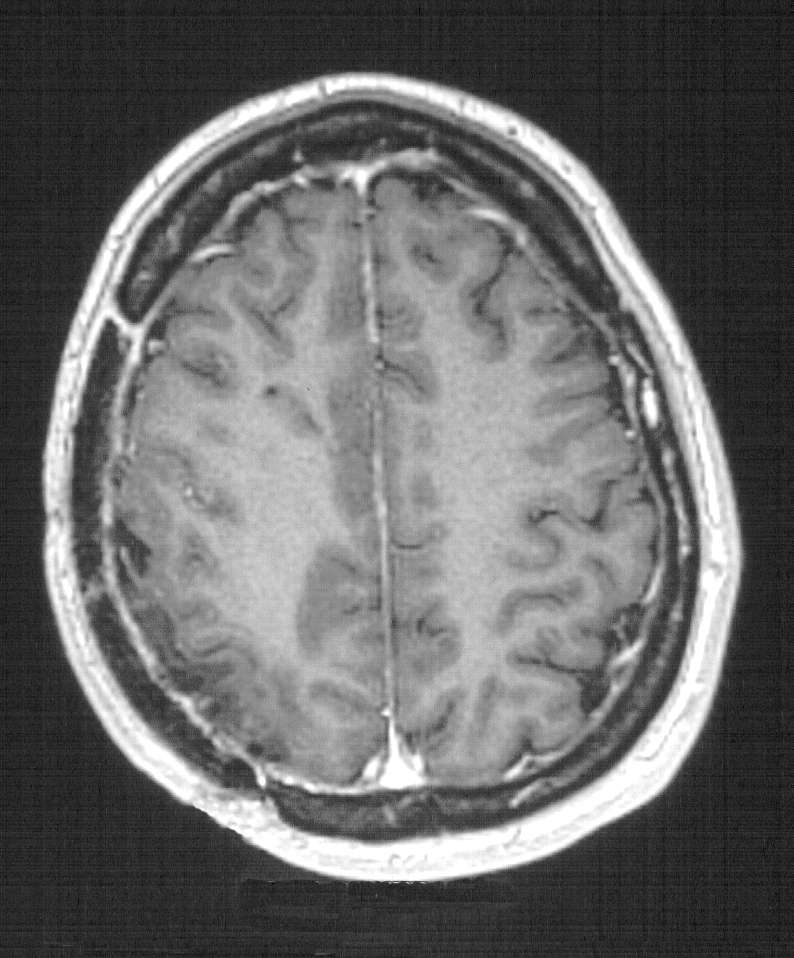
Un attento monitoraggio neuroradiologico fa rivelare spesso, a distanza di settimane o mesi, la scomparsa della falda ematica ed un’ottimale riespansione parenchimale (Figura 2).
 |
 |
|
Figura
2. TC encefalica nella seconda giornata post-operatoria.
Modesta falda ematica extradurale di tipo ex-vacuo. RM encefalo a
qualche mese di distanza dall'intervento di cranioplastica.
Completa riespansione parenchimale con scomparsa della falda
ematica sottotecale. |
Se la sostanza cerebrale è depleta, si può assistere ad un compenso volumetrico con una sottostante dilatazione ventricolare che porterà, comunque, la corteccia cerebrale a parete.
Fistola liquorale epicranica
Se vi è stata apertura durale per contemporanea rimozione di un tumore prima dell’apposizione della protesi cranica o lacerazione durale durante la fase di scollamento, il verificarsi di una fistola liquorale epicranica è sempre in agguato. In questi casi è sconsigliato ricorrere a delle medicazioni compressive tipo “turbante”.
In alternativa, ogni chirurgo ha il suo metodo. Può trovare del razionale l’inserzione, per qualche giorno, di un cateterino di derivazione liquorale a livello spinale e/o il posizionamento, temporaneo, di un sottile ago cannula a livello sottocutaneo, collegandolo a circuito chiuso con un sacchetto di raccolta.
Solitamente, in pochi giorni, si assiste all’attecchimento dei tessuti molli alla superficie della cranioplastica.
Come favorire lo scollamento per un successivo intervento di cranioplastica
Soprattutto in traumatologia cranica con ampia craniolacunia residua, il chirurgo può già predisporre il cratere osseo al meglio per accogliere il successivo impianto protesico.
a) Realizzare un perimetro osseo privo di angoli. La craniectomia dovrebbe essere ad ampio raggio di curvatura e non presentare spigoli.
b) I bordi dovrebbero essere conformati a “becco di flauto”, ovviamente, con il perimetro più ampio in superficie e quello più stretto in profondità.
c) Fra dura e piani sottocutanei può essere interposto un sottile foglietto di materiale sintetico che, impedendone l’adesione, consentirà un facile e rapido scollamento al tempo della cranioplastica. È stato proposto l’uso di un sottilissimo (0,1 mm) foglietto di polytetrafluoroethylene espanso (ePTFE) (Preclude® Peritoneal Membrane, W.L. Gore & Associates. Inc.). Questo materiale può essere anche risterilizzato. Va sottolineato che il chirurgo per utilizzare questi foglietti di materiale eterologo deve ritenere la ferita non potenzialmente infetta e deve prescrivere, comunque, una copertura antibiotica ad ampio spettro. La ferita chirurgica andrà monitorata affinché non sfuggano possibili eventi suppurativi.
Verifiche strumentali dell’avvenuto attecchimento e della colonizzazione delle cranioplastiche in idrossiapatite porosa
L’indagine strumentale più indicata ed accessibile è sicuramente la TC encefalica con risoluzione anche per osso. È però un esame che ci fornisce dati sul buon posizionamento della protesi, sulla buona solidificazione con i margini ossei, ma nulla ci dice sul processo di osteoinduzione della protesi stessa.
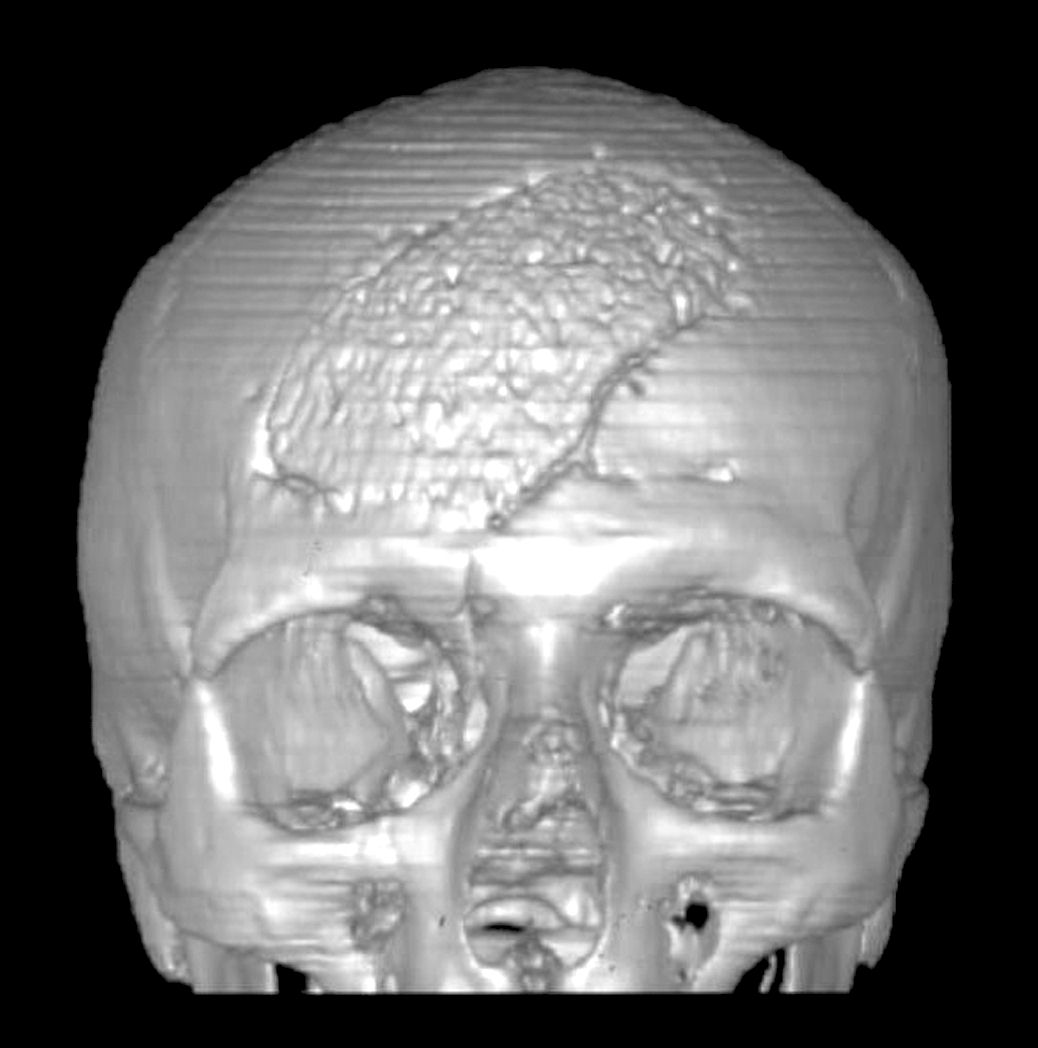
Si stanno conducendo studi mediante procedura di medicina nucleare per cercare di dimostrare in vivo, senza bisogno di prelievi bioptici, la progressione osteoblastica ed osteoclastica dalla periferia protesica verso il centro della stessa (Figura 3).
 |
|
|
|
Figura
3. Indagine scintigrafica eseguita con tecnica trifasica e
SPECT a livello della teca cranica. Nelle immagini tardive in
regione frontale destra (a sinistra nelle immagini), in
corrispondenza della protesi cranica, si rilevano significative
tracce di captazione del radiofarmaco, con ipercaptazione
periprotesica. Evidenza alle indagine TC 3D (immagine a sinistra)
dell'estensione della cranioplastica in idrossiapatite porosa
frontale destra. |
Il radiofarmaco utilizzato è il metilendifosfonato (MDP) legato al 99mTc che è un indicatore di attività osteoblastica. Nei casi studiati sono state eseguite immagini dinamiche precoci e statiche tardive anche con tecnica SPECT (tomografica) e misurazioni semiquantitative sulle regioni di interesse. Altri radiofarmaci di uso routinario che abbiano caratteristiche simili (possibilità di imaging con le comuni gamma camere, bassa tossicità, ridotta esposizione alle radiazioni ionizzanti) non sono attualmente disponibili. Non vi sono però ancora dati probanti. I risultati preliminari fanno rilevare che questa colonizzazione sembra verificarsi realmente anche se, per protesi particolarmente ampie, con tempi di progressione sicuramente più lenti di quanto fino ad ora stimato basandosi su delle deduzioni di tipo sperimentale.
Il problema di avere degli strumenti non invasivi per verificare l’osteoinduzione è emerso anche in un incontro sul tema tenutosi a Faenza il 5 aprile 2004. Nel tentativo di sfruttare al meglio le informazioni date dalla TC, F. Velardi, Neurochirurgo al Bambino Gesù di Roma sosteneva che “Il problema di non riuscire a capire, attraverso la TC, se è avvenuta o meno la fusione tra l’idrossiapatite e l’osso del Paziente, dopo 6-12 mesi dall’impianto, deriva dal fatto che l’acquisizione dei dati da parte della TC avviene pre-selezionando intervalli di intensità del segnale, in modo da poter discernere le ossa dagli altri organi, che comunque presentano densità differenti. Quindi viene selezionato un intervallo HU (Hounsfield Units, cioè l’unità di misura dell’intensità del segnale in termini di pixel), con un limite inferiore tale da non far vedere tutto ciò che non raggiunge quella determinata intensità di segnale. Questo va benissimo quando l’osso formato è di un adulto, quindi con uno spessore rilevante, ma non va più bene quando si prende in considerazione l’osso cranico di un bambino o un osso cranico in formazione. Quindi il consiglio è quello di diminuire il limite inferiore dell’intervallo di densità che viene acquisito e sceglierlo ad esempio pari a 140 HU - 1.400 HU, oppure 140 HU - 800 HU. Questa selezione deve essere fatta da parte del tecnico nel momento dell’acquisizione dei dati TC.”.
Come favorire l’attecchimento protesico
Vi sono evidenze sperimentali che il buon trofismo dell’opercolo osseo riposizionato è favorito dallo stretto contatto fra questo e la sottostante dura.
Per traslato, ciò può essere di contributo anche per l’attecchimento del manufatto in idrossiapatite porosa.
Pertanto, è raccomandabile una buona sospensione durale favorendo il più possibile un contatto fra la stessa e la superficie interna della cranioplastica. Inoltre, se possibile, è meglio evitare il posizionamento di estesi innesti di sostituti durali, specie se sintetici.
La protesi cambia colore
Quando viene consegnata in busta doppia, sigillata, di solito la cranioplastica in idrossiapatite è di colore tenuemente azzurrino.
Alle volte succede che dopo aver immerso per qualche decina di minuti il manufatto in soluzione antibiotica (solitamente rifampicina) questo diventi di intensità tendente al bianco sporco o giallo pallido-grigiastro. Nulla di preoccupante, si tratta di normali processi di interazione chimica che non alterano la qualità e la bontà della cranioplastica.

|
|
|
|
![]()